Апластическая анемия ― патология крови, которая связана с угнетением кроветворения (гемопоэза), в результате чего в костном мозге нарушается образованием эритроцитов, тромбоцитов и лейкоцитов.
Заболевание относится к одной из самых тяжелых видов анемии. Встречается преимущественно в молодом (5-25 лет) и пожилом (после 50 лет) возрасте. Радикальным методом терапии является пересадка костного мозга. При невозможности проведения операции, в большинстве случаев, прогноз для жизни неблагоприятный. Впервые описал заболевание иммунолог Пауль Эрлих в конце 19 века.
- Механизм развития (патогенез)
- Нарушение строения костного мозга (стромальная теория)
- Аутоиммунный конфликт в организме
- Преждевременное разрушение клеток (теория апоптоза)
- Классификация
- Причины
- Нарушения в генетическом материале (ДНК)
- Воздействие неблагоприятных факторов
- Химические вещества и радиация
- Лекарственные препараты
- Вирусные инфекции
- Симптомы
- Анемический синдром
- Геморрагический синдром
- Инфекционный синдром
- Наследственные апластические анемии
- Анемия Фанкони
- Анемия Даймонда-Блекфена
- Диагностика
- Дифференциальная диагностика
- Лечебная тактика
- Консервативная терапия (лекарственные препараты)
- Пересадка костного мозга (ПКМ)
- Костный мозг донора (аллогенная ПКМ)
- Кровь донора (аллогенное переливание клеток)
- Пуповинная кровь пациента (аутологичное переливание клеток)
- Костный мозг пациента и собственные стволовые клетки (аутологичная пересадка)
- Костный мозг однояйцевого близнеца
- Осложнения трансплантации костного мозга
- Это интересно!
- Профилактика
- Прогноз
- Частые вопросы пациентов
- Что необходимо запомнить
Механизм развития (патогенез)
Существует 3 теории развития апластической анемии, каждая из которых получила научное подтверждение. Воздействие нескольких неблагоприятных факторов утяжеляет течение болезни и затрудняет терапию. По статистике, анемия с угнетением кроветворения встречается редко ― в среднем у 2 человек на миллион населения.
Нарушение строения костного мозга (стромальная теория)
Костный мозг состоит из «скелета» — стромы, в котором находятся предшественники кровяных клеток. Здесь синтезируются факторы роста, которые стимулируют образование молодых клеток крови. Нарушение строения и функций костного мозга и его «скелета» возникает под действием генетических (мутаций хромосом) и приобретенных факторов. В результате развивается угнетение всех ростков гемопоэза: красного (эритроциты, тромбоциты) и белого (лейкоциты).
Аутоиммунный конфликт в организме
При некоторых условиях организм воспринимает собственные клетки костного мозга, как чужеродные, и вырабатывает защитные антитела. Это приводит к разрушению предшественников эритроцитов, тромбоцитов, лейкоцитов и, соответственно, уменьшению количества форменных элементов в крови.
Аутоиммунный конфликт возникает вследствие генетических мутаций. Это приводит к нарушению синтеза особых белков, при помощи которых организм распознает свои и чужие клетки. Сбой в работе иммунитета угнетает гемопоэз.
Преждевременное разрушение клеток (теория апоптоза)
В организме существует защитная система удаления поврежденных, мутированных и опухолеподобных клеток. Этот процесс называется апоптоз. Таким образом поддерживается нормальный клеточный состав тканей и осуществляется защита от онкологических заболеваний.
Под действием генетических факторов нарушается синтез белков, которые являются маркерами дефектных клеток. В результате апоптоз происходит в здоровом костном мозге. Это вызывает преждевременное разрушение молодых эритроцитов, тромбоцитов и лейкоцитов.

Классификация
В МКБ-10 апластической анемии присвоен код D61. Классификация включает причины (этиологию), вид угнетенного ростка гемопоэза, тяжесть течения заболевания.
По происхождению анемия бывает:
- врожденная (конституциональная) ― возникает вследствие генетических мутаций;
- приобретенная ― развивается при воздействии неблагоприятных факторов внешней среды;
- идиопатическая (первичная) ― происходит без видимой причины;
- неуточненная ― если при проведении диагностики этиологию не удалось установить.
По угнетенному ростку кроветворения выделяют анемии:
- истинные ― снижается образование всех клеток костного мозга (панцитопения);
- парциальные ― происходит угнетение только одного ростка кроветворения, чаще эритроцитарного.
Анемии по тяжести течения бывают:
- тяжелые ― нейтрофилы (вид лейкоцитов) 0,2-0,5х10*9/л, ретикулоциты (молодые формы эритроцитов) менее 1%, тромбоциты не более 20х10*9/л, при трепанобиопсии (пункция костного мозга для анализа) количество клеток составляет 50% от нормы;
- средней тяжести ― нейтрофилы более 0,5х10*9/л, ретикулоциты больше 1%, тромбоциты не менее 20х10*9/л, показатели трепанобиопсии ― 30%;
- сверхтяжелая ― нейтрофилов менее 0,2х10*9, анализ пунктата костного мозга ― менее 30%.
Апластической анемии легкой степени не существует. Заболевание всегда имеет тяжелое течение и сопряжено с риском развития осложнений.
Причины
Выделяют 2 основных фактора, которые приводят к возникновению апластической анемии. Это мутации хромосом и негативное влияние внешней среды (приобретенные формы болезни).
Нарушения в генетическом материале (ДНК)
Мутации в хромосомах вызывают врожденные анемии, которые обычно имеют тяжелое течение и сопряжены с пороками развития скелета и внутренних органов. Сюда относят анемию Фанкони, Даймонда-Блекфена, изменение крови при синдроме Дауна. Угнетение костного мозга происходит с самого рождения, поэтому заболевание трудно поддается консервативному лечению. Пересадка костного мозга (трансплантация) в большинстве случаев малоэффективна.
Воздействие неблагоприятных факторов
Приобретенные анемии развиваются под действием негативного влияния внешней среды. При своевременном выявлении болезни и предотвращения пагубного воздействия патологический процесс можно остановить и нормализовать работу костного мозга. Приобретенные анемии имеют более благоприятный прогноз, хорошо отвечают на проводимую терапию и трансплантацию костного мозга.
Химические вещества и радиация
Угнетение гемопоэза вызывают токсические продукты. Степень нарушения работы костного мозга зависит от длительности негативного влияния и дозы химического вещества. Высокой токсичностью обладают органические растворители, бензол, соединения мышьяка, пестициды. Отравление чаще происходит во время профессиональной деятельности, которая связана с контактом химических веществ, реже в быту. Влияние радиации (ионизирующего излучения) приводит к быстрому разрушению клеток крови и вызывает тяжелые формы апластической анемии.
Лекарственные препараты
Длительный прием медикаментов, токсичных для костного мозга, вызывает угнетение гемопоэза. Препараты оказывают прямое разрушающее влияние на клетки и опосредованное действие ― способствуют сбою в работе иммунной системы и выработке антител против предшественников форменных элементов крови. К токсичным для костного мозга относят некоторые транквилизаторы, антибиотики, противосудорожные, противомалярийные и антитиреоидные (применяют при повышенной функции щитовидной железы) средства, препараты золота, противоопухолевые лекарства.
Вирусные инфекции
Вирусные заболевания оказывают опосредованное действие на костный мозг путем развития аутоиммунных реакций против клеток-предшественников. Апластическая анемия в таких случаях развивается в течение полугода после перенесенного заболевания. Опасными для костного мозга являются вирусы гепатита В, С, D, ЦМВ (цитомегаловирус), Эпштейн-Барр, гриппа, папилломы человека.
В 50% случаев причину заболевания выявить не удается, анемию считают идиопатической или неуточненной.
Симптомы
Клинические признаки апластической анемии развиваются остро или могут возникать постепенно. Это зависит от причины заболевания и интенсивности воздействия на организм повреждающих факторов. При наследственных формах характерно медленное развитие патологии, в случае токсического воздействия химических веществ, радиации, медикаментов симптомы нарастают стремительно.
В начале заболевания возникает гипопластическая форма анемии, при которой ростки кроветворения угнетаются частично. Костный мозг сохраняет способность к образованию клеток, но в гораздо меньшем объеме. Апластический процесс подразумевает полное угнетение гемопоэза, что приводит к критическому снижению концентрации эритроцитов, тромбоцитов, лейкоцитов в крови.
Клиническая картина складывается из 3 синдромов: анемического, геморрагического, инфекционного. Синдром ― это совокупность симптомов, которые характерны для заболевания. Анемические и геморрагические проявления возникают первыми, затем присоединяются инфекционные осложнения. Степень тяжести клинических признаков зависит от причины болезни.
Анемический синдром
Возникает вследствие угнетения красного ростка гемопоэза. Снижается содержание эритроцитов, которые переносят кислород органам и тканям. При этом концентрация гемоглобина в клетках соответствует норме, так как в организме достаточно веществ для его синтеза. Вследствие низкого содержания эритроцитов развивается гипоксия (кислородное голодание тканей). Нормальная работа органов нарушается. Развивается хроническая недостаточность сердца, почек и печени. Страдает функция головного мозга.
Анемический синдром проявляется быстрой утомляемостью, слабостью, сонливостью. Возникает головокружение, частые головные боли, снижение остроты зрения и слуха, мелькание «мушек» перед глазами. Характерны перебои в работе сердца, которые сопровождаются тахикардией, неустойчивостью артериального давления, аритмиями, появлением шумов при выслушивании (аускультации) сердца.
Кожа становится сухая и бледная. Вследствие частых гемотрансфузий (переливаний крови) приобретает желтушный оттенок, что связано с гемолизом (разрушением) эритроцитов. Ухудшение обмена веществ из-за гипоксии приводит к расслоению ногтей, выпадению волос, разрушению зубной эмали. На голенях формируются долго незаживающие язвы.
Геморрагический синдром
Появляется вследствие нарушения образования предшественников тромбоцитов в красном ростке гемопоэза. Эти клетки отвечают за формирование сосудистых сгустков для остановки и предупреждения кровотечений. Чаще геморрагический синдром возникает сразу с анемическим или несколько позже. При редком заболевании ― амегакариоцитарной аплазии, угнетение образования тромбоцитов выходит на первый план, что может привести к ошибочному диагнозу.
Синдром характеризуется кровотечениями различной степени тяжести. Появляются мелкие и крупные кровоизлияния в коже ― геморрагическая сыпь. Склонность к возникновению синяков и гематом приводит к присоединению вторичной инфекции и нагноению. Характерны частые кровотечения из носа и десен, обильные менструации, увеличивается время остановки кровотечения. Кожа приобретает пятнистую окраску вследствие многочисленных синяков.
Прогрессирование болезни приводит к массивным кровотечениям из легких, желудка и кишечника. Кровоизлияние в головной мозг вызывает геморрагический инсульт и сопряжено с высоким риском смертельного исхода.
Инфекционный синдром
Угнетение белого ростка кроветворения приводит к нарушению образования лейкоцитов. Снижается количество сегментоядерных клеток (при рассмотрении под микроскопом в ядре заметны включения). К ним относят нейтрофилы (см. «Нейтропения»), базофилы (см. «Базопения») и эозинофилы (см. «Эозинопения»). Другие клетки лейкоцитарной формулы (моноциты, лимфоциты) обычно находятся на уровне нормальных показателей, а если рассматривать относительно сегментоядерных лейкоцитов, то их концентрация в крови повышается.
Так как белый росток кроветворения формирует иммунную защиту организма, в результате нарушается способность противостоять бактериальным и вирусным инфекциям, заражению гельминтами, образованию опухолей. Характерно тяжелое течение респираторных заболеваний, воспаление мочеполового тракта, легких. Часто возникают инфекции кожных покровов, долго не заживают царапины и раны. Повреждения кожи склонны к нагноению. Высокий риск развития сепсиса (заражения крови) ухудшает течение болезни.
Наследственные апластические анемии
Наиболее известные врожденные виды заболевания ― анемия Фанкони и Даймонда-Блекфена. Патологию выявляют в детском возрасте, чаще в 5-10 лет. При тяжелом угнетении кроветворения заболевание диагностируют в первые годы жизни.
Анемия Фанкони
Наследуется по аутосомно-рецессивному типу. Это означает, что генная мутация должна присутствовать у обоих родителей — только в этом случае патология проявится у детей. Но при этом вероятность рождения больного ребенка составляет 25%. Анемия Фанкони связана с нарушением синтеза белка в составе ДНК. В результате угнетается образование всех клеток крови в костном мозге.
Анемия сочетается с другими врожденными нарушениями. Характерна деформация черепа и скелета: маленький размер головы, укорочение больших пальцев рук, косолапость, низкорослость. Возникают пороки развития внутренних органов: почек (подковообразная форма, удвоение, образование множественных кист), половых органов (недоразвитие, отсутствие одного или обоих яичек), сердца (незаращение боталлова протока, деформация клапанов).
Часто встречается глухота, недоразвитие глаз, опущение века. Страдает умственное развитие. В зрелом возрасте анемия принимает злокачественное течение и трансформируется в рак крови (острый миелоидный лейкоз), который трудно поддается противоопухолевой терапии и сопряжен с высоким риском смерти.
Анемия Даймонда-Блекфена
Редкая форма заболевания, при которой происходит угнетение только эритроцитарного ростка гемопоэза. Наследуется по аутосомно-доминантному типу — для развития анемии достаточно мутации генов у одного из родителей. Вероятность появления болезни достигает 50%. Причина развития ― нарушение синтеза рибосомальных белков в хромосомах и нечувствительность костного мозга к эритропоэтину (веществу почек, которое стимулирует гемопоэз).
Анемию Даймонда-Блекфена диагностируют в первые годы жизни. В клинической картине преобладает анемический синдром: бледность кожи, слабость, головокружение, одышка, перебои в области сердца, низкая устойчивость к умеренным физическим нагрузкам.
У новорожденных могут выявлять пороки внутриутробного развития: незаращение верхней губы («заячья» губа), твердого неба («волчья» пасть), недоразвитие черепа и костей скелета, нарушение зрения (катаракта, слепота), пороки развития внутренних органов.
Диагностика
Для выявления апластической анемии назначают лабораторные и инструментальные методы обследования. В постановке диагноза учитывают клинические признаки, наследственность, факт влияния токсических веществ на организм. Стандарт диагностики ― лабораторные исследования крови и костного мозга. Анализы позволяют выявить угнетение гемопоэза и оценить тяжесть течения заболевания.
Таблица ― Лабораторная диагностика апластической анемии
| Показатель | Результат |
| Гемоглобин | Низкий уровень (ниже 110 г/л) |
| Эритроциты (красные кровяные тельца) | Ниже нормы (менее 2,5х10*12/л) ― эритропения |
| Гематокрит (соотношение жидкой части крови и форменных элементов) | Уменьшение уровня (ниже 30) |
| Ретикулоциты | Снижение показателя (0,2% и меньше) |
| Тромбоциты | Низкое содержание (менее 100х10*9/л) ― тромбоцитопения |
| Лейкоциты | Значительно ниже нормы (0,2-2,5х10*9/л) ― лейкопения |
| Зрелые нейтрофилы (сегментоядерные) Молодые нейтрофилы (палочкоядерные) | Менее 40% (при норме 50-72%) Ниже 2% (обычный показатель 6%) |
| Базофилы | Отсутствуют (в норме 0-1%) |
| Эозинофилы | Нет в крови или 1% (обычный показатель 1-5%) |
| Моноциты | Высокий показатель (более 8%) за счет относительного увеличения ― моноцитоз |
| Миелоциты (клетки-предшественники) | Появление в крови (в норме отсутствуют) |
| Лимфоциты | Высокий показатель (выше 40%) за счет относительного увеличения ― лимфоцитоз |
| Цветовой показатель (ЦП) ― степень насыщения эритроцитов гемоглобином | В норме (0,85-1,05) |
| Размер эритроцитов | Анизоцитоз (разного размера) |
| Форма красных кровяных телец | Пойкилоцитоз (необычная форма) |
| СОЭ (скорость оседания эритроцитов) | Выше нормы (более 20 мм/ч) при развитии инфекции |
| Эритропоэтин (гормон, который синтезируется почками и активирует гемопоэз) | Высокий показатель за счет компенсаторного увеличения при недостатке эритроцитов |
| Тимоловая проба (оценивает степень воспаления на фоне низкой функции иммунитета) | Увеличение показателя (норма 0-4) |
| Сывороточное железо | Обычный показатель Увеличение уровня микроэлемента вследствие частых гемотрансфузий |
| СРБ (С-реактивный белок) | Высокий уровень (более 20 мг/л) |
| Иммунология | |
| Антитела к ВИЧ-инфекции | Обнаруживают при заражении вирусом иммунодефицита человека |
| НBs-АГ и анти-HBc IgG (антитела против вируса гепатита В) | Положительный показатель при заражении инфекцией |
| Антитела к CMV (цитомегаловирусу)* | Отрицательные Положительные после перенесенной инфекции |
| Определение группы крови и резус-фактора | Необходимо для подбора донорской крови |
| Стернальная пункция (цитологическое исследование ― миелограмма) | |
| Предшественники эритроцитов и лейкоцитов | Отсутствуют |
| Молодые тромбоциты | Не выявляются или единичные |
| Трепанобиопсия (миелограмма и гистологическое исследование) | |
| Предшественники эритроцитов, лейкоцитов, тромбоцитов | Отсутствуют или находятся в критически малом количестве |
| Строма | Увеличение объема по сравнению с концентрацией клеток |
| Желтый костный мозг (неактивная часть гемопоэза) | Разрастается и преобладает над красным (активным) костным мозгом |
* Антитела к цитомегаловирусу определяют перед проведением гемотрансфузий. Если человек не заражен вирусом, ему переливают CMV-отрицательную кровь.
Стернальная пункция и трепанобиопсия являются обязательными методами обследования при апластической анемии. Только по анализам крови нельзя поставить точный диагноз. Стернальная пункция проводится путем прокола грудины на уровне 2-4 ребра полой иглой для забора небольшого количества костного мозга. Из полученного материала готовят 10-15 мазков на предметных стеклах для микроскопического исследования (изучения под микроскопом). В результате выявляют дефицит клеток в костном мозге.
Трепанобиопсию проводят путем прокола подвздошной кости (одной из костей таза). Методика позволяет взять больший объем костного мозга, провести не только цитологическое (изучение клеток), но и гистологическое исследование (оценку особенностей тканей). Кроме того, этот метод более надежный для диагностики на первых этапах развития болезни, когда остались островки нормального кроветворения. Если при стернальной пункции прокол попал на такой участок, то диагноз может быть ложно опровергнут. Обе процедуры делают под анестезией в условиях операционной.
Дополнительно назначают инструментальные методы обследования:
- УЗИ (ультразвуковое исследование) внутренних органов ― выявляет нарушение функции и врожденные пороки развития.
- ЭКГ (электрокардиограмма) ― исследование работы сердца, нарушения ритма и проводимости.
- КТ/МРТ (компьютерная и магнитно-резонансная томография) ― определяет нарушения в строении органов и новообразования.
- Рентгенография рук ― позволяет подтвердить врожденное недоразвитие костей.
- Генетические исследования ― оценивают риск развития анемии Фанкони и Даймонда-Блекфена.
Диагностику проводят в амбулаторных условиях. При тяжелом состоянии пациента и назначении пункции костного мозга дают направление на госпитализацию в гематологию.
Дифференциальная диагностика
В клинической практике чаще встречается приобретенная форма заболевания. Ее необходимо дифференцировать (отличать) от анемии Фанкони, лейкоза, В12-дефицитной анемии, миелодиспластического синдрома.
Таблица ― Дифференциальная диагностика
| Заболевание | Отличительные симптомы | Результаты обследования |
| Апластическая анемия приобретенная | Анемический синдром Кровотечения Частые и тяжелые инфекции Печень и селезенка не увеличены | Снижение в крови эритроцитов, лейкоцитов, тромбоцитов (панцитопения) Уменьшение клеток-предшественников в костном мозге |
| Анемия Фанкони | Пороки развития скелета и внутренних органов Пигментация (потемнение) кожи Детский возраст (5-12 лет) | Такие же, как при наследственной форме Фетальный гемоглобин в крови (характерный для внутриутробного развития) |
| Острый лейкоз (рак крови) | Увеличение печени и селезенки | Чаще угнетение одного ростка кроветворения (редко панцитопения) При проведении стернальной пункции ― опухолевые клетки |
| В12-дефицитная анемия | Нет геморрагического и инфекционного синдрома Поражение пищеварительного тракта и нервной системы | Макроцитоз в крови (большие размеры эритроцитов) В результатах стернальной пункции ― мегалобласты |
| Миелодиспластический синдром | Симптомы как при апластической анемии | В костном мозге нет дефицита клеток Генетические исследования выявляют характерные изменения хромосом |
Важный клинический признак заболевания ― отсутствие увеличения печени, селезенки и лимфатических узлов.
Лечебная тактика
В терапии апластической анемии применяют консервативные (медикаментозные) и оперативные методы. Лекарственные средства снижают агрессию иммунной системы против клеток костного мозга, устраняют воспаление, предупреждают развитие инфекций. Переливание крови временно восполняет недостаток клеток и улучшают общее самочувствие.
Единственным радикальным методом терапии, который может остановить развитие анемии, считают операцию по пересадке костного мозга от подходящего донора. Хирургическое лечение сопряжено с риском отторжения трансплантата и другими осложнениями, но дает шанс на выздоровление.
Консервативная терапия (лекарственные препараты)
Клинические рекомендации при апластической анемии включают иммуносупрессивные, заместительные и профилактические средства. Терапия направлена на поддержание кроветворения и улучшение общего самочувствия.
Таблица ― Лекарственные препараты при апластической анемии
| Цель терапии | Название препаратов | Способ применения |
| Иммунодепрессанты | ||
| Снижение аутоиммунной реакции в организме | Антилимфоцитарный глобулин (АЛГ) | 15 мг/кг в сутки в виде внутривенных инфузий (капельниц) для медленного введения Курс лечения ― 7-10 дней |
| Антитимоцитарный глобулин (АТГ) ― Атгам | 0,75 мг/кг в сутки внутривенно капельно медленно Курс терапии ― 7-10 дней | |
| Торможение апоптоза (преждевременного разрушения клеток) | Циклоспорин А (Сандиммун) | 5-10 мг/кг дважды в сутки Продолжительность лечения ― 3-12 месяцев |
| Глюкокортикоиды | ||
| Угнетение аутоиммунной и воспалительной реакции | Метилпреднизолон | Применяют высокие дозировки: 0,5-1 г в сутки в течение 5 дней |
| Заместительные средства* | ||
| Предупреждение кислородного голодания тканей | Переливание эритроцитарной массы | При уровне гемоглобина крови ниже 80 г/л |
| Профилактика кровотечений | Инфузии тромбоцитарной массы | При содержании клеток менее 50х10*9/л |
| Профилактические средства (антибиотики)** | ||
| Предупреждение инфекций и нагноения | Цефалоспорины (Цефазолин, Цефотаксим, Цефтриаксон) Макролиды (Эритромицин, Азитромицин, Спирамицин) Фторхинолоны (Ципрофлоксацин, Офлоксацин, Пефлоксацин) | Назначают в максимальных дозах в зависимости от тяжести течения инфекции |
| Профилактика грибковых заболеваний | Противогрибковые средства (Амфотерицин В, Бифоназол, Интраконазол, Миконазол) | Дозировки подбирают индивидуально |
| Дополнительные препараты | ||
| Стимуляция образования эритроцитов | Анаболические стероиды (Оксиметолон) | 200-300 мг в сутки в течение 1-3 месяцев |
| Активация белого ростка кроветворения (лейкоцитов) | Колониестимулирующий фактор (гранулоцитарный) | При уровне нейтрофилов не менее 0,5х10*9/л |
* Переливание лейкоцитов не проводят. Белые клетки крови быстро разрушаются и часто вызывают аллергические реакции.
** При высоком риске инфекции (гранулоциты менее 0,5х10*9/л) пациентов переводят в палаты с соблюдение стерильности. Ежедневно кожу обрабатывают антисептическими растворами, в рацион включают только термически обработанную пищу. Минимизируют количество инъекций для предупреждения нагноения кровоподтеков от укола иглой.
Пересадка костного мозга (ПКМ)
Для проведения операции необходимо подобрать подходящего донора, клетки которого способны прижиться в организме пациента. Для этого кровь больного (реципиента) и донора исследуют на совпадение по антигенному составу (особенностям строения белков форменных элементов крови).
Максимально совместимый костный мозг другого человека приживается в 70-80% случаев. Частичное совпадение по антигенам дает эффективность на 40-50%. После операции пациенту назначают длительный прием иммунодепрессантов для предупреждения отторжения пересаженного костного мозга.
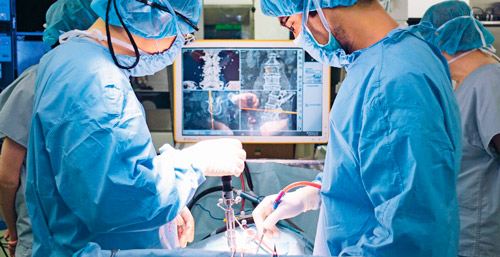
Прорывом в гематологии стала возможность использования собственные клетки крови. Забор биологического материала проводят до начала болезни. В таких случаях приживаемость костного мозга составляет 98%, нет опасности отторжения трансплантата и необходимости принимать иммунодепрессанты.
Таблица ― Оценка эффективности терапии
| Степень | Показатели крови |
| Полная ремиссия (восстановление функции костного мозга) | Нейтрофилы более 1х10*9/л Гемоглобин выше 100 г/л Тромбоциты более 100х10*9/л |
| Частичная ремиссия | Нейтрофилы 0,5-1,0х10*9/л Гемоглобин 80-100 г/л Тромбоциты 20-100х10*9/л |
| Отсутствие эффекта | Нет значимых изменений в клеточном составе крови Необходимость в регулярных гемотрансфузиях |
В зависимости от особенностей операции выделяют несколько видов трансплантации: аллогенную и аутологичную. В первом случае пересадку биологического материала проводят от донора. Во втором ― применяют собственные ткани пациента.
Костный мозг донора (аллогенная ПКМ)
Донором клеток может стать родственник больного. По статистике, только в 30% случаев удается найти подходящего по всем показателям человека в близком окружении пациента. Пол и возраст не имеют значения. Забор костного мозга можно делать даже у грудного ребенка. Если не удалось найти донора среди родственников, совместимый костный мозг ищут в банке органов. Поиск может занять месяцы и годы.
По сути, операцию проводят только донору, у которого извлекают костный мозг. Для этого под наркозом делают трепанобиопсию. После забора костного мозга (700-1000 мл) клетки переливают реципиенту посредством внутривенных инфузий.
Кровь донора (аллогенное переливание клеток)
Забор костного мозга при помощи трепанобиопсии можно заменить менее травматичной методикой. Клетки-предшественники (стволовые клетки) получают путем взятия крови у донора. Затем биологический материал обрабатывают в специальных аппаратах и переливают реципиенту.
Получение клеток-предшественников из крови, а не из костного мозга имеет ряд преимуществ. После операции посредством трепанобиопсии восстановление кроветворения донора длится в течение года. Полученные клетки путем обработки крови не вызывают тяжелых иммунных реакций у реципиента, а реабилитация донора сокращается до 3-4 недель.
Пуповинная кровь пациента (аутологичное переливание клеток)
После рождения ребенка делают забор крови из пуповины (соединительного канала между плацентой и плодом). Биологический материал консервируют и помещают в специальные хранилища. При необходимости пуповинную кровь можно использовать, если человек затем заболевает апластической анемией или онкологическими заболеваниями.
Методика эффективно используется последние десятилетия. Собственные стволовые клетки не отторгаются и не вызывают иммунный конфликт. Единственный недостаток ― высокая стоимость хранения крови в банке донорских органов.
Костный мозг пациента и собственные стволовые клетки (аутологичная пересадка)
В период стойкой ремиссии и восстановления функции гемопоэза больному проводят трепанобиопсию или получают стволовые клетки из крови. При возникновении обострения биологический материал можно использовать для эффективного и безопасного лечения.
Костный мозг однояйцевого близнеца
В организме близнецов, которые развивались из одной яйцеклетки, антигены клеток крови максимально похожи. Пересадка костного мозга в таких случаях приравнивается к использованию собственных тканей.
Осложнения трансплантации костного мозга
После пересадки костного мозга могут возникать инфекционные, трансплантационные и функциональные нежелательные последствия. Нагноение операционной раны и остеомиелит (гнойное воспаление кости) встречаются редко, так как во время операции соблюдаются стерильные условия.

Гораздо чаще возникает отторжение трансплантата. Иммунная система воспринимает пересаженный костный мозг, как чужеродное вещество, и синтезирует против него антитела. Чем меньше антигенных совпадений между кровью донора и реципиента, тем выше риск развития осложнений.
Операция по пересадке костного мозга становится серьезным испытанием для организма. Если работа функциональных систем уже была нарушена до вмешательства, то риск нарушения их работы повышается в десятки раз. Усугубляет ситуацию прием высоких доз иммунодепрессантов, которые направлены на профилактику отторжения трансплантата. Лекарственные средства обладают токсичностью и ухудшают функцию органов. Развивается почечная и печеночная недостаточность.
Это интересно!
Новаторским методом терапии апластической анемии является применение колониестимулирующих средств ― ростовых факторов. Это синтетические препараты, которые способны активировать кроветворение. Ростовые факторы улучшают функцию стромы костного мозга, нормализуя рост и созревание клеток-предшественников крови.
Самым популярным и хорошо изученным считают гранулоцитарный колониестимулирующий фактор. Он активирует белый росток гемопоэза. В результате в крови увеличивается количество лейкоцитов, снижается риск возникновения тяжелых инфекций и гнойных осложнений. Препараты, содержащие гранулоцитарный фактор: Лейкостим, Граноцит, Нейпоген.
Такое лечение помогает пациентам нормализовать состав крови и общее состояние, улучшить качество жизни до пересадки костного мозга. Терапия обладает высокой эффективностью, редко вызывает тяжелые побочные явления. Относительный недостаток препаратов ― высокая цена, если учитывать, что лечение может продлиться долгие месяцы и даже годы.
Профилактика
Предупреждение развития анемии направлено на устранение неблагоприятных факторов внешней среды (профессиональных и бытовых вредностей, радиации), необоснованного назначения токсичных для костного мозга препаратов. Это первичная профилактика болезни. Сюда же входит предупреждение и своевременное лечение инфекций.
Вторичная профилактика проводится при уже возникшем заболевании. Пациенты нуждаются в диспансерном наблюдении гематолога, регулярном обследовании и получении поддерживающего лечения.
Прогноз
Продолжительность и качество жизни зависит от причины анемии, тяжести течения, возникновения осложнений, сроков пересадки костного мозга. После проведения операции прогноз благоприятный в 40-98% случаев. Выздоровление наиболее вероятно после пересадки собственных стволовых клеток.
Неблагоприятный прогноз чаще возникает при наследственных формах, остром течении и быстром прогрессировании болезни. Смертельный исход наступает вследствие массивных кровотечений и тяжелых инфекций, которые плохо поддаются антибактериальной терапии.
Частые вопросы пациентов
Вопрос: Можно ли вылечить апластическую анемию?
Ответ: Единственным радикальным способом терапии является пересадка костного мозга или стволовых клеток. Эффективность операции выше, если биологический материал берут у самого больного. В таких случаях вероятность выздоровления высокая. Если пересаживают донорский костный мозг, то эффективность операции снижается за счет высокого риска отторжения клеток и необходимости длительного приема токсических иммунодепрессивных препаратов.
Вопрос: Апластическая анемия ― это рак крови или нет?
Ответ: Онкологические заболевания возникают вследствие появления в организме атипичных клеток, которые быстро растут и разрушают нормальные ткани. Рак крови вызывает формирование таких клеток в костном мозге. При апластической анемии происходит обеднение кроветворения. В костном мозге находятся нормальные клетки, но в критически малом количестве. Апластическая анемия ― тяжелое заболевание, но это не рак.
Вопрос: Какую диету лучше использовать?
Ответ: В питание включают повышенное содержание белков и углеводов, ограничивают поступление жиров. Рекомендуют диетическое мясо (индюшатина, телятина, курятина), рыбу (пеленгас, карп, хек, минтай), морепродукты. Каши, фрукты и овощи поставляют в организм сложные углеводы, которые медленно всасываются и пополняют энергетические запасы организма. Из рациона исключают маргарин, сало, свинину, баранину, колбасные изделия, копчености, полуфабрикаты, фастфуд. Для улучшения аппетита в пищу добавляют специи.

Вопрос: Можно лечить заболевание народными средствами?
Ответ: Апластическая анемия относится к тяжелой патологии крови, которая трудно поддается терапии лекарственными препаратами. Зачастую помочь больному может только пересадка костного мозга. Народные средства неэффективны в борьбе с болезнью.
Вопрос: Когда используется и какая эффективность препарата Атгам?
Это иммунодепрессивный препарат, который устраняет разрушающее действие иммунитета на собственные клетки костного мозга. Представляет собой антилимфоцитарный глобулин, приготовленный из крови лошади.
Предназначен для внутривенного введения. Назначается одновременно с другими иммунодепрессантами ― глюкокортикоидами и циклоспорином. Атгам эффективен при отсутствии показаний к пересадке костного мозга, нормализует кроветворение, улучшает общее состояние, увеличивает продолжительность жизни.
Что необходимо запомнить
Апластическая анемия связана с угнетением всех ростков кроветворения, что приводит к критическому снижению содержания эритроцитов, тромбоцитов и лейкоцитов. Это одна из самых серьезных форм малокровия (обо всех видах читайте здесь), по тяжести сопоставимая с онкологическими заболеваниями.
Что важно запомнить:
- Анемия бывает наследственная и приобретенная. Своевременное устранение негативных факторов может остановить развитие патологии. При наследственной форме болезни это сделать невозможно, поэтому врожденные анемии обычно протекают тяжело с неблагоприятным прогнозом.
- Клинические проявления тяжелые, связаны с нарушением функции органов, кровотечениями, затяжными инфекциями. Это приводит к развитию осложнений с высоким риском смертельного исхода.
- Для диагностики недостаточно проведения анализа крови, обязательно назначают пункцию костного мозга. Изучение миелограммы выявляет панцитопению (уменьшение количества клеток всех ростком кроветворения).
- Лечение проводят иммунодепрессивными средствами, что сопряжено с развитием побочных эффектов. Выздоровление обычно наступает после пересадки костного мозга.
- Пациенты должны находиться на диспансерном учете у гематолога. Это предупреждает быстрое прогрессирование болезни.
Тяжесть течения заболевания и прогноз зависят от своевременной диагностики и терапии. Чем раньше начато лечение, тем больше шансов остановить опасную для жизни патологию.